Chimica | I gas ideali
Gli studi condotti nel tempo su vari tipi di gas ci consentono di affermare che, dal punto di vista macroscopico, tutti i gas si comportano in modo pressoché identico. Il loro comportamento si differenzia molto da quello delle sostanze liquide e solide: i gas sono infatti molto sensibili alle variazioni di temperatura e di pressione.
La teoria cinetico-molecolare utilizza un particolare modello di gas, chiamato gas ideale o perfetto, le cui particelle (atomi o molecole) presentano le seguenti caratteristiche:
1. Sono puntiformi, per cui il loro volume è trascurabile rispetto a quello effettivamente occupato da tutto il gas;
2. Non si attraggono reciprocamente e sono separate da spazio vuoto;
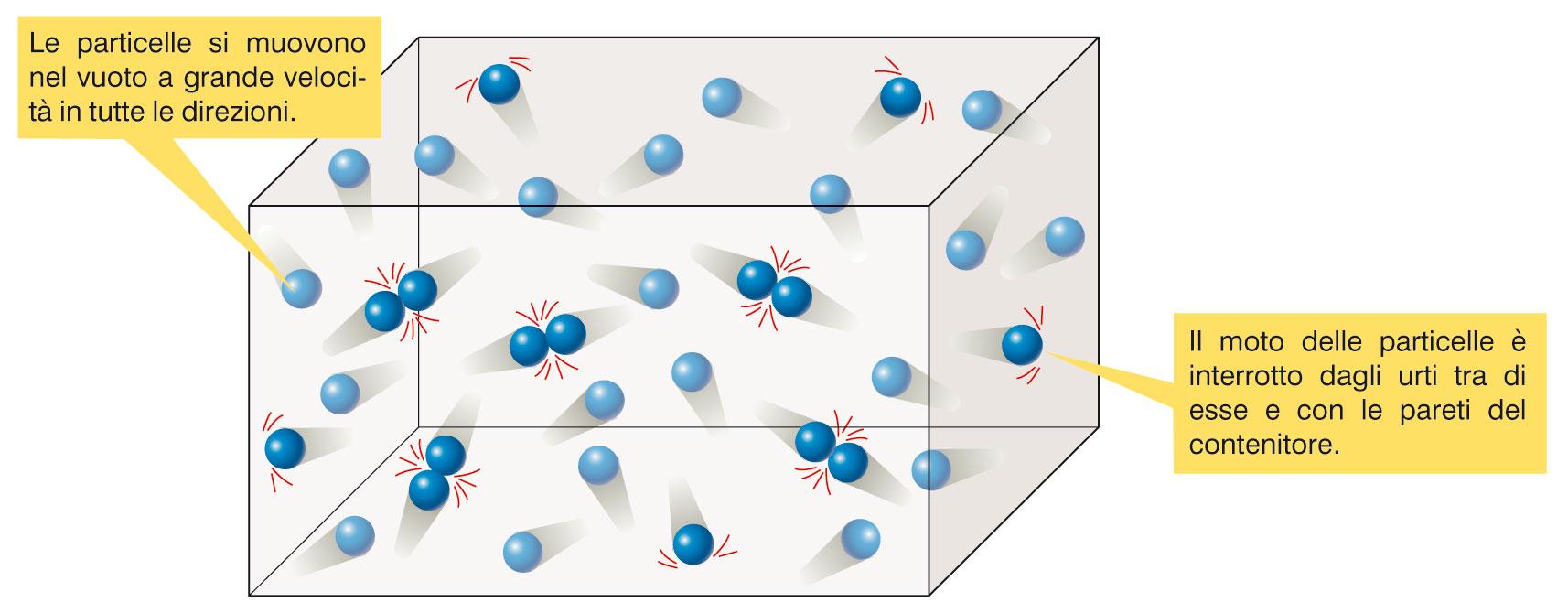
3. Si muovono in modo caotico e a grande velocità in tutte le direzioni; se considerate all’interno di un ipotetico contenitore, il loro moto rettilineo viene interrotto da urti fra le particelle stesse e con le pareti del contenitore; tali urti sono elastici, e le particelle si comportano come palline di gomma perfettamente elastiche, cioè non provocano una dispersione di energia.
Un gas è caratterizzato da tre grandezze fisiche: pressione, temperatura e volume.
- La pressione di una gas è il risultato del continuo impatto delle molecole del gas sulle pareti
del recipiente che le contiene. - La temperatura assoluta di un gas è proporzionale all’energia cinetica media delle sue molecole.
Il modello del gas ideale è in grado di descrivere bene il comportamento dei gas reali quando sono piuttosto rarefatti e si trovano a una temperatura molto maggiore di quella di liquefazione. In tal caso, infatti, le particelle sono così lontane le une dalle altre che il volume occupato dalla massa gassosa è grandissimo, ma prevalentemente vuoto.